新皇冠肺炎爆发以来,相关有效治疗药物的发现和临床试验的进展备受关注。在2月19日新发布的《新型冠状病毒诊断与治疗方案(试验六版)》(以下简称“试验六版诊断与治疗方案”)中,除了以前版本中提到的α-干扰素、洛匹那韦/利托那韦(商品名“Crezhi”)和利巴韦林外,抗病毒治疗的试验药物已正式添加到之前多次提到的磷酸氯喹和阿比多中。与此同时,许多治疗新诊断肺炎的药物正在开发或临床试验正在进行中,包括最近受到关注的拉德克利夫和法比亚韦等。另一方面,企业作为相关药品的主要供应商,也在关注其技术研发和生产供应。
\r下面结合新发布的第六版诊疗方案和公众信息,对上述潜在有效治疗药物的背景、临床试验进展、研发和生产企业进行梳理。
\r需要注意的是,目前对于新诊断的肺炎还没有明确有效的药物释放。上述药物只是初步显示疗效或潜在有效性。临床试验仍在进行中。一些药品的有效性和安全性仍不确定,相关企业的业务影响也不确定。
\rlopinavir/ritonavir
\r洛匹那韦/利托那韦是由艾伯维公司开发的抗艾滋病药物。它已在中国上市,主要用于治疗成人和2岁以上儿童的艾滋病毒感染。根据公开信息,洛匹那韦/利托那韦在体外研究中对传染性非典型肺炎冠状病毒和多囊卵巢综合征冠状病毒具有抑制作用。洛匹那韦/利托那韦也是从诊断和治疗计划的第一版到第六版推荐的抗病毒试验药物。
\r据了解,目前,除了原来的研究制造商艾伯维以外,世界上的洛匹那韦/利托那韦制造商还包括仿制药巨头迈兰(Mylan,宣布与辉瑞制药的普强合并)和印度第二大仿制药工厂西普拉(Sipura)
\r对于国内企业而言,目前a股上市公司科伦药业已开始研发该药物。科伦制药在2月17日发布的一份声明中表示,该公司已经完成了洛匹那韦/利托那韦片剂配方技术的研发,进入生产线大规模试生产阶段,预计将于3月初实现批量生产。
\rα-干扰素
\rα-干扰素是一种广谱抗病毒药物,以前主要用于治疗儿童呼吸道病毒感染。从诊断和治疗计划的第一版到第六版,干扰素α被推荐为抗病毒治疗试验药物。
\r据了解,在国内上市公司中,安科生物技术正在进行全负荷生产。此外,根据公开信息,许多企业,如中国医药集团公司和无名制药也在生产干扰素-α
\r利巴韦林
\r利巴韦林是一种广谱、强效的抗病毒药物,在第五版诊断和治疗计划中推荐作为抗病毒试验药物,并在第六版诊断和治疗计划中继续试验。在诊断和治疗计划中,建议将利巴韦林与干扰素或洛匹那韦/利托那韦联合使用。
\r在国内上市公司中,诚信药业、延安碧康等企业有利巴韦林生产批准文件
\r其中,诚信制药在2月8日的公告中表示,该公司拥有利巴韦林原料药和制剂
\r延安碧康公司于2月11日晚宣布,公司已收到延安市人民政府《关于延安碧康公司办理利巴韦林注射液等药品委托生产手续的批复》,拟投资500万元支持公司子公司利巴韦林注射液等药品的生产。
\r氯喹磷酸盐
\r磷酸氯喹是一种已上市多年的抗疟药。它是新皇冠肺炎诊断和治疗中的“旧药新用”。2月21日上午,科技部副部长徐南平在国务院联防联控机制新闻发布会上表示,在京、粤两省共检测出氯喹磷酸酯135例,其中普通型130例,重症型5例。到目前为止,还没有从轻型或普通型转为重型,4例重型患者出院,1例重型患者转为普通型,整体效果良好。在新发布的第六版诊断和治疗计划中,首次推荐将磷酸氯喹作为抗病毒药物进行试验。
\r据了解,国内有20多家企业持有氯喹磷酸酯生产批准文件,涉及白云山、石爻集团、昆药集团、上海药、精华药、芸香药业、华北制药等上市公司。然而,由于其主要用于疟疾预防和治疗,近年来其市场份额相对较低,实际生产商相对较少。
\r芸芸制药有限公司早些时候宣布公司已经获得氯喹磷酸酯片的生产许可,但已经多年没有生产和销售该片。已获得该药品的补充申请批准,并组织恢复生产。同时,公司作为临床研究合作单位,积极参与氯喹磷酸酯片治疗新型冠状病毒的临床研究
\r白云山近日宣布,公司控股子公司广州白云山光华制药有限公司已收到广东省药品监督管理局核发的《磷酸氯喹片药品补充批准文件》,将及时恢复磷酸氯喹片的生产,并经检验合格后上市。
\r据公开信息,广药集团、精华素制药和中药也在积极恢复磷酸氯喹片的生产。
\rAbidor
\r阿比多是由前苏联药物化学研究中心开发的广谱抗病毒药物。它主要用于治疗流感。据媒体报道,李兰娟院士团队此前的研究发现,阿比多可以在体外细胞实验中有效抑制冠状病毒。目前,在新发布的第6版诊断和治疗计划中,推荐使用阿比多作为抗病毒试验药物。
\r生产企业中,香港上市公司史思耀集团2月19日宣布,该公司生产的阿比朵尔原料药及制剂,其阿比朵尔胶囊已被纳入多省市防疫产品库存或防控药品绿色通道。
\r江苏吴中在早前发布的风险预警公告中称,盐酸阿比多片是该公司全资子公司江苏吴中药业集团有限公司生产和销售的产品之一。2019年1月至9月,医药集团盐酸阿比多片销售收入为1620.8万元,占上市公司营业收入的1.06%。
\r众所周知,西姆契尔·阿比朵尔盐酸分散片正在生产和供应。
\rridgeway
\rRidgeway是美国吉利公司开发的抗埃博拉病毒感染的药物。国外的临床试验尚未完成。在中国进行的体外实验表明,瑞奇韦对新冠状病毒有较好的抑制作用和安全性。在2月21日上午举行的国务院联防联控机制新闻发布会上,科技部副部长徐南平表示,针对瑞奇威的临床试验已纳入200多例重症和危重病患者,30多例轻、常见病患者,但盲症尚未发现。
\r在中国上市公司中,博瑞药业、海南海药、科龙药业已经成功仿制或正在进行相关研发。
\r其中,博瑞医药于2月11日晚宣布,公司已成功复制开发了里德四维原料药的合成工艺和制备工艺,并已批量生产里德四维原料药,里德四维原料药的批量生产正在进行中。
\r海南海药于2月14日晚宣布,公司已完成瑞西韦原料药及制剂技术的研发和第一批瑞西韦制剂的生产,年生产能力350万单位。
\r科伦药业2月12日在互动平台上表示,与瑞奇威相关的研究工作已经开始。目前,工艺开发和放大研究正在全面展开,进展顺利。可以大量生产的样品将很快获得。
\r此外,湖南华纳制药有限公司2月6日在官方网站上披露,该公司在解决关键问题上取得了突破性进展,抄袭了瑞特·四维的技术。
\rfabiravir
\rfabiravir是一种用于治疗流感的药物,已在国外上市。最初的研究企业是富山化学工业有限公司科技部生物中心主任张新民2月15日表示,对于新诊断的肺炎,法比亚韦最初显示出明显的疗效和较低的不良反应。在2月21日上午举行的国务院联防联控机制新闻发布会上,科技部副部长徐南平表示,费边拉维尔在深圳进行了80次对照试验,目前效果良好。然而,fabiravir尚未被正式纳入新冠状肺炎的诊断和治疗计划。
\r在国内上市公司中,海正制药于2月16日晚宣布,该公司已于2016年6月与原法比睿研究药物公司日本福山化学工业有限公司签署了化合物专利独家许可协议。目前,公司已获得国家食品药品监督管理局批准发布的产品《药品注册批准文件》和《药品临床试验批准文件》。
\r据科技部副部长徐南平介绍,21日,4名接受干细胞治疗的重症患者已出院,并将进一步扩大临床试验。
\r国际方面,据公开报道,世界卫生组织总干事谭德赛在最近于内华达州总部举行的例行记者会上表示,世界卫生组织R&D蓝图将洛匹那韦/利托那韦和里奇韦列为对抗新冠状病毒的关键疗法,两种疗法的临床试验的初步结果预计将在三周内公布。
\r附件:
\r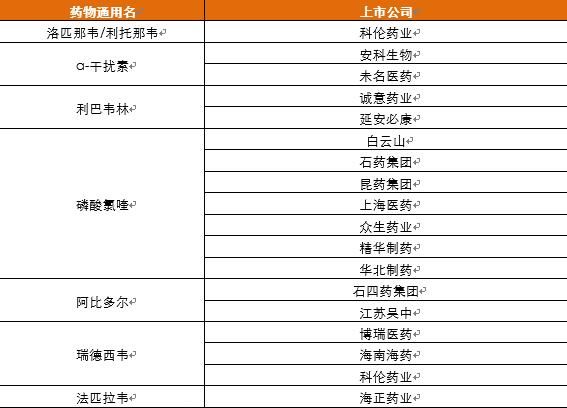
制表:上市公司财务来源研究所:上市公司公告及其他公共信息