![[合成氨工业的核心反应]工业合成氨反应:N2+3](http://img.lookmw.cn/yuedu/170612/427190_48.jpg)
[合成氨工业的核心反应]工业合成氨反应:N2+3
1048x786 - 170KB - JPEG

已知25℃时合成氨反应的热化学方程式为:N2(g
515x238 - 71KB - PNG

如图所示.合成氨反应:N2(g)+3H2(g)2NH3(g)△
264x203 - 9KB - JPEG
的量A.B混合于2L的密闭容器中.发生如下反应:
380x263 - 18KB - PNG

合成氨工业中.下列措施有利于提高平衡转化率
111x284 - 12KB - PNG

在一定条件下.合成氨反应达到平衡后.混合气体
381x255 - 19KB - JPEG

合成氨是人类科学技术上的一项重大突破.其反
673x337 - 38KB - JPEG

合成氨反应的热化学方程式为:N2(g)+3H2(g)2N
485x261 - 12KB - PNG
![[选修-化学与技术]合成氨工业的主要反应为:N2](http://thumb.1010pic.com/pic5/upload/201310/52839b21d7819.png)
[选修-化学与技术]合成氨工业的主要反应为:N2
191x240 - 11KB - PNG
![[合成氨工业的核心反应]工业合成氨反应:N2+3](http://img.lookmw.cn/yuedu/170612/427190_63.jpg)
[合成氨工业的核心反应]工业合成氨反应:N2+3
1037x778 - 126KB - JPEG
![[合成氨工业的核心反应]工业合成氨反应:N2+3](http://img.lookmw.cn/yuedu/170612/427190_46.jpg)
[合成氨工业的核心反应]工业合成氨反应:N2+3
1069x802 - 209KB - JPEG
![[合成氨工业的核心反应]工业合成氨反应:N2+3](http://img.lookmw.cn/yuedu/170612/427190_58.jpg)
[合成氨工业的核心反应]工业合成氨反应:N2+3
1069x802 - 104KB - JPEG
![[合成氨工业的核心反应]工业合成氨反应:N2+3](http://img.lookmw.cn/yuedu/170612/427190_61.jpg)
[合成氨工业的核心反应]工业合成氨反应:N2+3
1069x802 - 85KB - JPEG
![[合成氨工业的核心反应]工业合成氨反应:N2+3](http://img.lookmw.cn/yuedu/170612/427190_49.jpg)
[合成氨工业的核心反应]工业合成氨反应:N2+3
1026x770 - 149KB - JPEG
![[合成氨工业的核心反应]工业合成氨反应:N2+3](http://img.lookmw.cn/yuedu/170612/427190_59.jpg)
[合成氨工业的核心反应]工业合成氨反应:N2+3
1026x770 - 59KB - JPEG
简介:合成氨别名氨气,分子式NH3。是指由氮和氢在高温高压和催化剂存在下直接合成的氨。世界上的氨除少量从焦炉
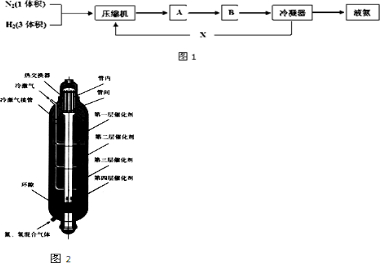
合成氨反应原理为:N2△H=-92.4kJ?mol-1一种工业合成氨的简易流程图如图1所示:(1)步骤Ⅱ中制氢气原理如下:①CH4△H=+206.4kJ?mol-1②CO+H2(g)△H=-41.2kJ?mol-1对于
B 【解析】试题分析:A、t1时正反应速率比原来增大,可能是升高了温度,也可能是增大了压强,还可能是增大了反应物质的浓度,错误;B、t2时没有渐变过各,对于反应前后化学计量
德国化学家哈伯1909年提出了工业氨合成方法,即"循环法",这是目前工业普遍采用的直接合成法。反应过程中为解决氢气和氮气合成转化率低的问题,将氨产品从合成反应后的气体中分离出来,未反应气和新鲜氢氮气混合重新参与合成反应。合成氨反应式如下: N2+3H2=2NH3 合成氨的主要原料可分为固体原料、液体原料和气体原料。经过近百年的发展,合成氨技术趋于成熟,形成了一大批各有特色的工艺流程,但都是由三个基本部分组成,即原料气制备过程、净化过程以及氨合成过程。 将纯净的氢、氮混合气压缩到高压,在催化剂的作用下合成氨。氨的合成是提供液氨产品的工序,是整个合成氨生产过程的核心部分。氨合成反应在较高压力和催化剂存在的条件下进行,由于反应后气体中氨含量不高,一般只有10%~20%,故采用未反应氢氮气循环的流程。氨合成反应式如下: N2+3H2→2NH3(g) =-92.4kJ/mol 国际上有关的研究成果认为,温和条件下的固氮作用一般包含以下三个环节: ①络合过程。它是用某些过渡金属的有机络合物去络合N2,使它的化学键削弱;②还原过程。它是用化学还原剂或其他还原方法输送电子给被络合的N2,来拆开N2中的N-N键;③加氢过程。它是提供H+来和负价的N结合,生成NH3。
正反应速率减小的倍数小于逆反应速率减小的倍数``错``应该是 大于 3H2 +N2 =2NH3 系数大``变化就大```所以正反应速率减小的倍数大于逆反应速率减小的倍数
习题“已知某条件下,合成氨反应的数据如下:N2(g)+3H2(g)2NH3(g)起始浓度/mol·L-11.03.00.22s末浓度/mol·L-10.61.81.04s末浓度/mol·L-10.41.21.4当用氨.”的分析与解答
习题“工业合成氨反应:N2+3H22NH3,在一定条件下已达到平衡状态.(1)若降低温度,会使上述平衡向生成氨的方向移动,生成每摩尔氨的反应热数值是46.2KJ/mol,则该反应的热化
(1)25℃时,合成氨反应的热化学方程式为: (g)△H=-92.4kJ/mol ①在该温度时,取lmolN 放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是_92.4kJ.(填“小于”,“
合成氨的反应方程式 下载作业帮 扫二维码下载作业帮 4亿+用户的选择 下载作业帮安装包 扫二维码下载作业帮 4亿+用户的选择 合成氨的反应方程式 作业帮用户2017-10-23
N2和H2反应生成NH3的反应为可逆反应,反应为:N2+3H2 2NH3,可逆反应不能完全进行到底,反应物的转化率不能达到100%,此温度下的1molN2和3molH2放在一密闭容器中,不能