今年12月1日是第32个世界艾滋病日,宣传主题是“社区与众不同”,宣传主题是“社区动员抗击艾滋病,健康中国和我们的行动”。
艾滋病人艾滋

据统计,全世界每年有170万人感染人类免疫缺陷病毒(艾滋病毒)。他们被迫终生接受抗逆转录病毒疗法,否则将面临致命艾滋病的风险。
目前,3 790万艾滋病毒感染者(PLWH)中有2 230万人接受了抗逆转录病毒疗法,这使他们的预期寿命接近正常水平。然而不幸的是,这些药物只能到此为止。它们无法到达病毒休眠多年的细胞。此外,这些药物潜在的长期不良反应仍然未知。
脆弱时段:关键的第一天
当艾滋病毒开始传播时,它不会立即扩散到全身。它必须首先在本地繁殖(主要在生殖组织中)。只是在最初的局部扩张之后,病毒才开始传播。这种局部扩张在病毒有效建立系统性感染之前提供了一个非常短的脆弱窗口期。
艾滋病人艾滋
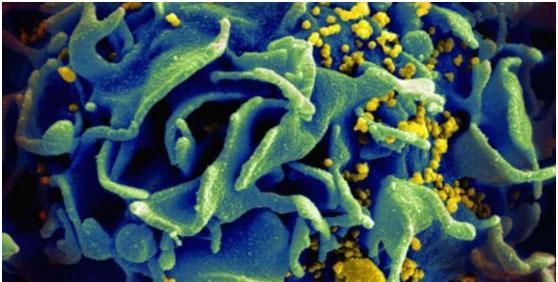
免疫系统的反应就像一场武装斗争:敌人入侵,身体自卫。病毒是入侵者,而白细胞是试图守住堡垒的士兵。白细胞有自己的“步兵单位”:淋巴细胞、吞噬细胞、粒细胞等。吞噬细胞群有一个更特殊的单位叫做“浆细胞样树突细胞”。这些小圆细胞在体内巡逻,负责病原体检测和抗病毒反应的协调。换句话说,他们是告密者和发起整个辩护过程的人。当他们发现威胁时,他们会改变形状,长出叫做树突的突起。科恩解释道:“最重要的是,它们开始产生大量干扰素,这是一种能在其他细胞中引起抗感染的蛋白质。”
顾名思义,艾滋病毒优先以免疫系统为目标:它攻击并削弱身体自身的防御系统,感染者对最轻微的感染变得敏感。一旦艾滋病病毒到达,它将清除PDCs并阻止他们发出警报。“这种病毒似乎不会直接杀死它们,但它会让它们以一种人们仍然不理解的方式消失,”人类反病毒学研究单位的高级研究员范说。"没有感染部位和系统性PDCs有助于建立感染."
抗艾滋病病毒感染的人源化小鼠模型
科恩说:“考虑到艾滋病毒对PDC的影响,我们想知道如果我们在感染前和感染期间提高PDC的水平和功能会发生什么。”为了证实这一点,科学家们使用了一种叫做Flt3受体配体的特殊蛋白质来刺激人类小鼠骨髓中PDCs的产生。这些啮齿动物被设计成具有人类免疫系统来代替老鼠的免疫系统。因此,艾滋病毒在感染的人类小鼠中的行为与在人类宿主中的行为相同。
施用这种特殊蛋白将使这些小鼠的PDCs水平保持在高水平,并产生一些显著的结果:1 .感染小鼠的初始数量减少;2.检测血液中病毒所需的时间已经延长;3.血液中的病毒量,也称为病毒血症,显著减少。范指出:“我们观察到病毒血症减少了100倍,换句话说,通过维持高水平的PDCs抑制了最初的感染。”
对艾滋病毒疫苗设计的影响
这项开创性的工作还表明,Flt3受体配体的注射不仅增加了PDC的丰度,而且增强了它们检测病毒和检测后产生干扰素的能力。
当然,艾滋病毒感染通常不会被注意到,当检测到病毒血症时,已经有点太晚了。在这种情况下,科恩和范的发现在预防和潜在治疗方面非常重要。科恩说:“这些新发现现在对艾滋病毒疫苗的设计至关重要。这种疫苗的基本目标是教导免疫系统通过引入一种弱化的艾滋病毒来保护自己。我们现在可以把重点放在PDCs上,在感染的早期控制病毒的传播和扩散。”